Progetto Scientifico 2017
Progetto Scientifico 2017 “quelli che…con LUCA onlus” sostenuto presso i Laboratori “M. Tettamanti” e “S.Verri” di Monza.
Trattamento della Leucemia Mieloide Acuta Refrattaria o Recidiva dopo trapianto di midollo tramite l’uso di linfociti T killer modificati per esprimere recettori chimerici specifici (CARs)
Introduzione e razionale dello studio
Nonostante gli attuali regimi chemioterapici assicurino una remissione completa nel 65-75% dei casi di Leucemia Mieloide Acuta (LMA) in pazienti di età inferiore ai 60 anni, la sopravvivenza globale ai cinque anni è inferiore al 30%, con una prognosi peggiore per i pazienti più anziani, raggiungendo meno del 10% , a causa di un alto tasso di recidiva.
L’immunoterapia tramite l’utilizzo di linfociti T geneticamente modificati per esprimere i recettori chimerici (CARs) rappresenta una nuova ed innovativa frontiera terapeutica, come recentemente dimostrato nel trattamento della Leucemia Linfoblastica Acuta (LLA).
Nel contesto della LMA, la terapia con linfociti T modificati con i CAR (CAR-T) è ad oggi ancora una sfida, e solo pochi studi pre-clinici in Cina ed America hanno raggiunto le prime fasi sperimentali in clinica.
Negli ultimi anni il gruppo di Ricercatori del lab. Tettamanti ha sviluppato, tramite studi in vitro e in vivo, due CAR diretti contro due diversi bersagli di leucemia mieloide, CD33 e CD123, per modificare geneticamente le cellule CIK, o cellule killer indotte da citochine, un particolare tipo di linfociti T facilmente espandibili in vitro.
L’obiettivo finale del presente studio è lo sviluppo di un protocollo di fase I/II per valutare la fattibilità e la tossicità di cellule CIK modificate con il CAR-CD33 per il trattamento di pazienti con LMA refrattaria o per il trattamento di pazienti con recidiva di malattia, quindi in ricaduta dopo il trapianto di midollo.
In particolare, le cellule CIK verranno modificate attraverso un sistema di manipolazione genica non virale, recentemente ottimizzato dal gruppo dei nostri Ricercatori, e successivamente testate in vitro e in vivo.
In parallelo, al fine di disegnare una futura terapia che non comporti una potenziale mieloablazione a lungo termine nei pazienti trattati con Cellule killer, verrà investigata la possibilità di modificare le stesse per renderle ancor più sicure.
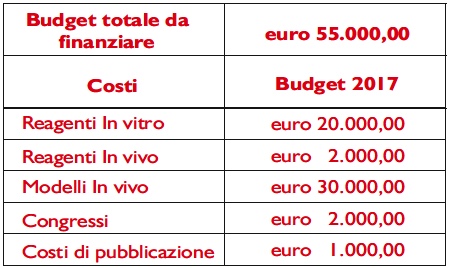
Piano di sviluppo e budget necessario per le attività pre-cliniche in vitro e in vivo
Obiettivi anno 2017
- Generazione tramite sistema non virale e caratterizzazione in vitro di cellule CIK-CAR-CD33
- Caratterizzazione in vivo dei profili di efficacia delle cellule CIK-CAR-CD33
Messa a punto di un modello murino per testare l’attività delle cellule CIK-CAR-CD33 contro linee cellulari di LMA resistenti al trattamento chemioterapico.